Для коллоидных растворов характерно движение частиц дисперсной фазы, вызываемое беспорядочными ударами со стороны молекул среды, находящихся в тепловом движении (броуновское движение). Это придает системе кинетическую устойчивость, которая состоит в том, что концентрация коллоидных растворов одинакова по всему объему системы и при правильном хранении не изменяется во времени.
В процессе хранения золи переходят в гели, при этом мицеллы не разрушаются, а просто связываются друг с другом, образуя свободные ячейки, внутри которых сохраняется вода. Гель можно высушить и получить твердый коллоид.
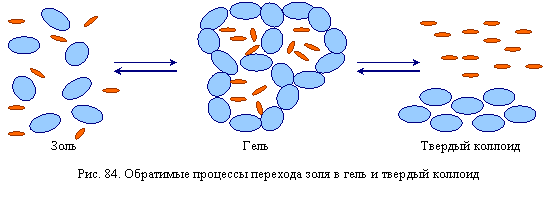
Переход золь 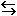 гель
гель 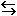 твердый коллоид практически всегда обратим.
твердый коллоид практически всегда обратим.
Устойчивость золя можно нарушить, устранив одноименный заряд коллоидных частиц и защитную гидратную оболочку. На границе раздела коллоидная частица – среда устанавливаются два равновесия:
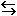 противоионы в среде (1);
противоионы в среде (1);
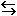 вода в среде (2).
вода в среде (2).
Если сместить равновесие (1) влево (←), то возрастет число противоионов в коллоидной частице и уменьшится её заряд. Уменьшение заряда частицы приведет к уменьшению числа молекул воды в гидратной оболочке, то есть к смещению равновесия (2) вправо (→). Устойчивость системы нарушится. Можно сместить равновесие так, что частица станет незаряженной, частицы перестанут отталкиваться и слипнутся, укрупнятся. Такой процесс называется коагуляцией. Коагуляция приводит к потере кинетической устойчивости, которая выражается в образовании осадка – седиментации.
Рассмотрим схему нарушения устойчивости коллоидного раствора на примере золя Fe(OH)3.
Строение мицеллы:
{[m Fe(OH)3· n Fe3+·3(n – x) Cl-·y H2O]3x+ + 3x Cl- · z H2O}.
На границе раздела фаз существует два равновесия:
3 (n – x) Cl- 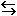 3x Cl- (1)
3x Cl- (1)
y H2O 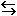 z H2O (2)
z H2O (2)
Коагуляция связана со смещением равновесий (1) влево (←) и (2) вправо (→). Состав при этом изменится: частицы теряют заряд и защитную гидратную оболочку:
{[m Fe(OH)3· n Fe3+·3 Cl-]0},
нейтральные частицы коагулируют и образуют осадок.