
Рис. 6.4 |
Одним из наиболее характерных свойств жидкого состояния является наличие резкой границы между жидкостью и ее паром.
Рассмотрим поведение жидкости, помещенной в закрытый сосуд и заполняющей часть его объема (рис. 6.4).
В этом случае резкая граница между жидкостью и паром разделяет два состояния, или, как говорят, две фазы вещества, из которых газообразная, как уже отмечалось, характеризуется гораздо меньшей (в тысячи раз) плотностью, чем жидкая. В жидкой фазе среднее расстояние между молекулами много меньше (в десятки раз), чем в паре, и в соответствии с этим молекулярные силы взаимодействия в жидкости гораздо больше, чем в паре.
Конечно, и в паре, и в жидкости молекулы находятся в непрерывном движении и могут покидать жидкость, переходя в пар. Понятно, что не исключен и обратный переход молекул – из пара в жидкость. Процесс перехода молекул из жидкости в пар называется испарением. Обратный переход молекул из пара в жидкость – конденсацией.
Если процессы перехода молекул из жидкости в пар и их обратного возвращения в жидкость взаимно компенсируются, то наступает состояние динамического равновесия. Пар, находящийся над поверхностью жидкости, помещенной в закрытый сосуд, в этом случае становится насыщенным. Однако между насыщенным паром и жидкостью сохраняется резкая граница. Обмен молекулами не нарушает равновесия между двумя этими состояниями, хотя это равновесие имеет подвижный характер.
Процесс установления такого равновесия сводится к следующему. Покидающие жидкость молекулы должны преодолеть силы притяжения со стороны других молекул, совершив при этом некоторую работу. Кроме того, они должны совершить работу против внешнего давления, созданного ранее образовавшимся паром. Вся эта работа может быть совершена только за счет кинетической энергии теплового движения молекул. Понятно, что в процессе испарения могут участвовать не все молекулы, а только те из них, которые обладают достаточной кинетической энергией для совершения указанной выше работы. Очевидно, что процесс испарения, в ходе которого жидкость покидают наиболее быстрые молекулы, сопровождается значительными энергетическими затратами. Справедливость этого вывода убедительно подтверждается примерами из повседневной жизни. Так, выйдя из воды после купания, мы ощущаем прохладу, а тот факт, что при испарении воды, налитой в стакан, мы не замечаем понижения ее температуры, объясняется тем, что вода в процессе испарения получает теплоту из окружающей среды.
Совершенно ясно, что процесс испарения жидкости можно сделать более интенсивным, повышая температуру жидкости за счет внешних источников тепла или увеличивая площадь ее свободной поверхности, поскольку испарение будет происходить тем эффективнее, чем сильнее преобладает процесс ухода молекул из жидкости над обратным процессом.
Число молекул, возвращающихся в жидкость в процессе конденсации, прямо пропорционально числу молекул в паре. Поэтому для ускорения процесса испарения следует принять меры по уменьшению числа молекул, возвращающихся назад в жидкость. Например, при ветре молекулы, вылетевшие из жидкости, относятся в сторону и тем самым уменьшается вероятность их обратного возвращения в жидкость. Именно поэтому на ветру мокрые вещи высыхают быстрее.
Если процесс испарения жидкости происходит в закрытом сосуде, то рано или поздно в системе установится динамическое равновесие, при котором количества пара и жидкости будут оставаться постоянными. Установившаяся при этом плотность пара соответствует определенному давлению. Это давление называется упругостью насыщенного пара. Понятно, что с повышением температуры упругость насыщенного пара должна возрастать, поскольку при более высоких температурах число быстрых молекул, покидающих жидкость, увеличивается, а следовательно, для того чтобы установилось равновесие между процессами испарения и конденсации, должна увеличиться и упругость насыщенного пара. Таким образом, с повышением температуры упругость насыщенного пара возрастает.
Уже отмечалось, что если жидкость испаряется без изменения температуры, то к ней нужно подводить тепло. Количество тепла, которое нужно подвести для того, чтобы изотермически испарить определенное количество жидкости при внешнем давлении, равном упругости насыщенного пара, зависит от природы жидкости и называется скрытой теплотой испарения. Эта величина может быть рассчитана на единицу массы, либо на моль жидкости. В первом случае она называется удельной, во втором – молярной скрытой теплотой испарения. Рассмотрев физический механизм процесса испарения, можно без труда заключить, что скрытая теплота испарения является количественной характеристикой сил межмолекулярного взаимодействия в жидкости. Очевидно, что чем эти силы больше, тем больше скрытая теплота испарения.
Процесс конденсации, связанный с переходом молекул из пара в жидкость, должен сопровождаться выделением энергии. На основании закона сохранения энергии можно утверждать, что скрытая теплота конденсации должна быть равна скрытой теплоте испарения.
Скрытая теплота испарения экспериментально определена для большого числа жидкостей. Существует ряд методов для определения этой величины. Одним из наиболее распространенных является метод, в основу которого положена экспериментальная зависимость давления насыщенного пара от температуры. Теоретически установлено, что эта зависимость имеет вид:
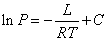 , , |
(6.10) |

Рис. 6.5 |
 от
от 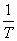 позволяет определить значение
величины
позволяет определить значение
величины  , из которой без труда определяется
скрытая теплота испарения.
, из которой без труда определяется
скрытая теплота испарения.
В одинаковые открытые сосуды налейте одинаковые массы холодной и горячей воды и выставьте сосуды на мороз. Не удивляйтесь, если горячая вода замерзнет раньше. Попытайтесь объяснить, почему?