Рассмотрим термодинамическую систему, представляющую собой один моль идеального газа, которая изменяет свое состояние в условиях различных изопроцессов.
1. Изохорический процесс (V = const). Работа в этом процессе, как следует
из (4.16), равна нулю. Процесс сводится к теплообмену системы с окружающей средой.
Первый закон термодинамики при этом условии принимает вид:
Как следует из (4.22), количество теплоты, полученное системой, если она
представляет собой один моль идеального газа, равно
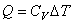 . . |
(4.26) |
Поскольку
CV > 0 для всех веществ, то знаки
Q и Δ
Т
совпадают. При
Q > 0 (энергия подводится к системе) температура системы
повышается, т.е. Δ
Т > 0, при
Q < 0 система охлаждается,
т.е. Δ
Т < 0.
Если в состав системы входит ν молей идеального газа, то равенство (4.26)
представляется в виде:
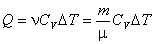 , , |
(4.27) |
где
m – масса газа, μ – его молекулярная масса.
2. Изобарический процесс (Р = const). На основании определения теплоемкости
(4.20) количество теплоты Q, подведенное к системе в изобарном процессе,
для одного моля идеального газа равно:
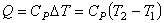 . . |
(4.28) |
Поскольку для любой системы
CP > 0, то при
Q > 0
(система получает энергию извне) Δ
Т > 0 и
Т2 >
T1, система нагревается.
При
Q < 0 (система отдает энергию окружающей среде) Δ
Т < 0,
Т2 <
T1, система охлаждается. Уравнение (4.28) для ν молей идеального
газа записывается в виде:
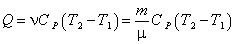 . . |
(4.29) |
Найдем работу, которую совершает система в изобарическом процессе, переходя из состояния 1 в состояние 2. Начальное и конечное состояния системы описываются уравнениями
| PV1 = RT1, PV2 = RT2, |
(4.28) |
из которых следует
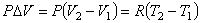 . . |
(4.30) |
Обобщение равенства (4.30) для случая молей в системе приводит к результату:
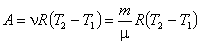 . . |
(4.31) |
3. Изотермический процесс. При изотермическом процессе температура системы
не изменяется (ΔТ = 0), а, следовательно, ее внутренняя энергия, являясь
для идеального газа только функцией температуры, остается постоянной, то есть ее
изменение ΔU = 0. Это значит, что сообщаемое системе количество теплоты
идет на совершение работы.
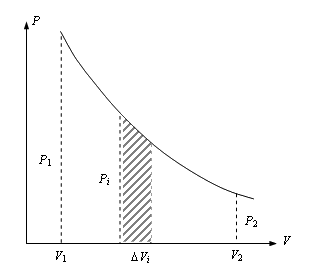
Рис. 4.9
|
Найдем работу расширения моля идеального газа в изотермическом процессе.
Изотерма в координатах Р – V представляется гиперболой (рис. 4.9).
Как уже было рассмотрено ранее, работу расширения газа от начального
объема V1 до V2 можно найти, используя равенство (4.17):
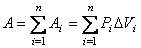 . . |
|
Давление моля идеального газа, как следует из уравнения состояния, равно
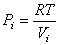 . . |
|
и выражение для работы принимает вид:
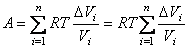 . . |
(4.32) |
Очевидно, что чем меньшие интервалы изменения объема ΔVi
выбираются для вычисления работы, тем точнее будет получено ее значение.
Предельный переход в соотношении (4.32) приводит к выражению:
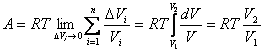 , , |
(4.33) |
где
V1 и
V2 – объемы, занимаемые системой соответственно в начальном и конечном
состояниях. Обобщая формулу (4.33) на случай системы, содержащей ν молей газа,
получаем равенство:
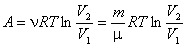 . . |
(4.34) |
Пользуясь уравнением изотермического процесса (PV = const),
равенство (4.34) можно представить через другие параметры состояния системы:
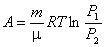 , , |
(4.35) |
где
Р1 и
Р2 – давление газа в начальном и
конечном состояниях.
4. Адиабатический процесс. Адиабатический процесс – процесс, идущий без теплообмена с окружающей средой. Это значит, что система должна быть теплоизолирована, либо процесс должен протекать так быстро, что за время процесса не происходит теплообмена системы с окружающей средой. Условие адиабатичности процесса означает, что Q = 0.
Уравнение первого закона термодинамики для адиабатического процесса принимает вид:
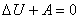 . . |
(4.36) |
Из последнего соотношения следует, что
А = – Δ
U и для
одного моля идеального газа равно
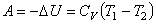 . . |
(4.37) |
Из (4.37) очевидно, что если адиабатически изолированная система подвергается
сжатию (внешние силы совершают над системой работу, поэтому работа отрицательна),
то Δ
U > 0. Это означает, что адиабатическое сжатие идеального
газа приводит к повышению его температуры. Напротив, адиабатическое расширение
идеального газа (работа совершается самой системой, поэтому она положительна)
может происходить только за счет уменьшения его внутренней энергии (Δ
U < 0),
поэтому температура газа при его адиабатическом расширении должна понижаться.
Все рассмотренные выше процессы могут быть представлены одним уравнением –
уравнением политропического процесса. Политропический процесс – это процесс,
идущий с постоянной теплоемкостью. Уравнение политропического процесса имеет вид
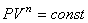 , , |
|
где
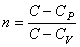
– показатель политропы.
Уравнения всех рассмотренных процессов, их графики, значения теплоемкости и
показатели политропы, а также значения всех величин, входящих в выражение
первого закона термодинамики, представлены в таблице 4.1.
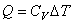 .
.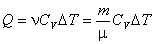 ,
,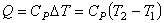 .
.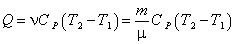 .
.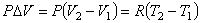 .
.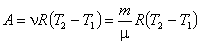 .
.
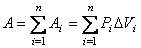 .
.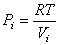 .
.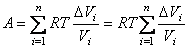 .
.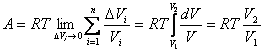 ,
,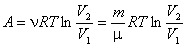 .
.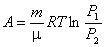 ,
,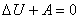 .
.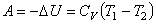 .
.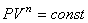 ,
,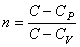 – показатель политропы.
– показатель политропы.